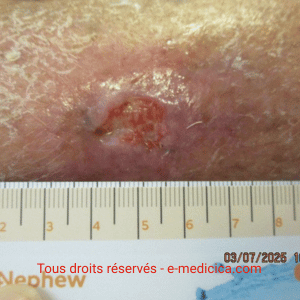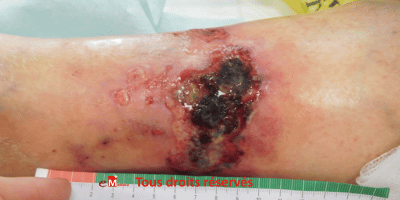
Angiodermite nécrotique (ulcère de Martorell) : signes, diagnostic, traitement
L’angiodermite nécrotique est un type d’ulcère ischémique particulièrement douloureux du membre inférieur, souvent confondu avec d’autres plaies chroniques de jambe. Cette pathologie, encore trop souvent méconnue, nécessite une prise en charge spécifique et rapide. Découvrez comment l’identifier, la différencier et la traiter efficacement en pratique clinique, la greffe restant le traitement le plus efficace.
Qu’est-ce que l’angiodermite nécrotique ?
L’angiodermite nécrotique (aussi appelée « angiodermite nécrosante », « ulcère de Martorell », « ulcère suspendu », « ulcère hypertensif », vasculopathie livedoïde) est une plaie cutanée ischémique liée à une microangiopathie artériolaire des membres inférieurs. Elle est due à une occlusion des petites artères du derme, dans un contexte d’hypertension artérielle ancienne, parfois de diabète ou d’insuffisance veineuse chronique.
Quelle est la cause de l’angiodermite nécrotique ?
L’origine précise de cette maladie reste mal connue : on suspecte un rôle central des atteintes vasculaires (microangiopathie hypertensive), mais d’autres facteurs sont probablement impliqués.
Quel est le terrain de l’angiodermite nécrotique ?
Bien que l’angiodermite nécrotique soit souvent présentée comme une maladie rare, elle peut représenter jusqu’à 10 à 15 % des ulcères de jambe dans certaines études. Elle atteint en priorité les femmes de plus de 65 ans, mais peut aussi toucher les hommes. Le terrain vasculaire est constant : hypertension artérielle ancienne, diabète, parfois insuffisance veineuse. La bilatéralité et la symétrie sont possibles : une même lésion peut se développer sur les deux jambes. Il n’y a jamais d’angiodermite nécrotique au-dessus du genou ou au niveau du pied.
Quels sont les signes cliniques typiques ?
- La lésion démarre généralement après un traumatisme minime à la jambe.
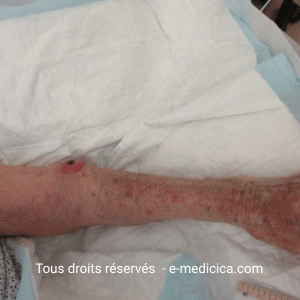
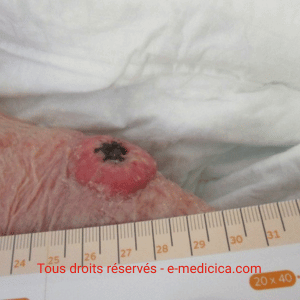
- Elle débute par une rougeur, évolue vers un aspect violacé, puis une nécrose cutanée avec formation rapide d’une ulcération extrêmement douloureuse.
- La douleur est d’emblée intense et permanente, même la nuit, sans position de soulagement.
- L’ulcération s’étend de façon centrifuge, à partir d’une bordure rouge et violacée (livédo).
- L’évolution peut être aggravée par le frottement ou une détersion agressive, traduisant un phénomène de pathergie.
Comment diagnostiquer l’angiodermite ?
Le diagnostic est avant tout clinique.
À l’examen, la plaie est nécrosée, à bords nets, peu exsudative, souvent localisée sur la partie antéro-externe du tibia, parfois de manière bilatérale et symétrique. Elle peut aussi se situer en regard de la zone achilléenne (exemple : suite à un frottement sur le talon d’une chaussure). La périphérie violacée (« livédoïde ») est caractéristique.
Un bilan doppler artériel des membres inférieurs est indispensable : il permet d’exclure une artérite sévère.
Quelle est la place de la biopsie ? Elle est proposée en cas de doute diagnostic.
Quels sont les diagnostics différentiels ?
- Ulcère artériel : terrain d’artériopathie, localisation plutôt au pied ou aux orteils, absence de microangiopathie
- Pyoderma gangrenosum : ulcère très inflammatoire, bords violacés, contexte de maladie systémique
- Ulcères veineux : bords irréguliers, exsudat abondant, douleur moins intense
- Nécrose cutanée d’autres origines : calciphylaxie en cas d’insuffisance rénale chronique sévère
Le patient peut parfois avoir une insuffisance veineuse associée ou une artériopathie oblitérante des membres inférieures mais celle-ci ne doit pas être suffisamment sévère pour expliquer la présence de l’angiodermite nécrotique.
Tableau résumé des diagnostics différentiels
| Diagnostic | Localisation | Douleur | Terrain | Aspect de la plaie |
|---|---|---|---|---|
| Angiodermite nécrotique | Tibia antéro-externe mais jamais au dessus du genou et au niveau du pied | Intense, permanente | Femme >65 ans, HTA, diabète | Nécrose noire, bords nets, extension centrifuge, livedo périphérique |
| Ulcère artériel | Pied, orteils, suspendu | Intense | Artériopathie | Nécrose sèche, creusante |
| Pyoderma gangrenosum | Jambe, périostéal | Variable | Maladie systémique | Bords violacés, très inflammatoire |
| Ulcère veineux | Plutôt malléolaire | Modérée | Insuffisance veineuse | Bords irréguliers, exsudat |
| Calciphylaxie cutanée | Jambe, cuisse | Très douloureux | IRC sévère | Nécrose, calcifications sous-cutanées |
Quels sont les facteurs favorisants ?
L’angiodermite nécrotique est surtout liée à une microangiopathie hypertensive, secondaire à une HTA ancienne. Les facteurs de risque : hypertension artérielle, diabète, âge avancé, insuffisance veineuse, obésité.
Des facteurs favorisants : traumatisme même minime, friction, parfois gestes de soins inadaptés (détersion agressive). Attention à la calciphylaxie cutanée chez les patients en insuffisance rénale chronique sévère : le diagnostic différentiel est parfois difficile.
Comment soigner une angiodermite nécrotique ?
Séquence du traitement
- Repos +++ et traitement efficace de la douleur (antalgiques palier II/III) en premier lieu
- Greffe précoce +++ : traitement principal, permettant un soulagement rapide de la douleur et un arrêt de la poussée
- Soins locaux : pansements doux, éviter toute friction ou détersion agressive (phénomène de pathergie).
- La douche n’est pas contre-indiquée, à condition de respecter un faible débit
- Compression non recommandée
- Contrôle strict de la tension artérielle et correction des facteurs de risque cardiovasculaires
- Traitements complémentaires possibles : corticoïdes topiques forts, thérapie par pression négative, PRP en gel, matrices dermiques, anticoagulants (en cours d’évaluation), électrothérapie (prometteuse)
- Prévention des complications : surinfection : prélèvement bactériologique, antibiothérapie adaptée si besoin
- Prise en charge pluridisciplinaire (médecin, infirmier expert en plaies, dermatologue, chirurgien plasticien)
Quelles sont les indications d’hospitalisation ?
L’hospitalisation est souvent nécessaire en cas de lésion étendue ou de douleur incontrôlable.
La stratégie thérapeutique dépend de l’ancienneté de la plaie et de la réponse au traitement. Des traitements spécialisés peuvent être nécessaires pour obtenir la cicatrisation complète.
Suivez ma formation pour établir une stratégie adaptée.
Quelles sont les complications possibles et l’évolution ?
Comme toute plaie chronique, l’angiodermite nécrotique expose à plusieurs complications :
- Surinfection bactérienne : le risque de surinfection locale est élevé, surtout chez les patients fragiles. Un prélèvement bactériologique est indiqué devant tout signe clinique d’infection.
- Douleur chronique invalidante : la douleur peut persister longtemps et altérer la qualité de vie, nécessitant parfois une prise en charge antidouleur spécialisée.
- Retard de cicatrisation : certaines lésions évoluent lentement malgré une prise en charge optimale, notamment en cas de terrain défavorable (diabète, âge avancé).
- Extension ou récidive : l’ulcère peut s’étendre de façon centrifuge, ou réapparaître sur l’autre jambe (atteinte bilatérale possible).
- Exposition tendineuse ou osseuse possible selon les localisations
- Risque d’amputation : exceptionnel mais possible en cas d’évolution défavorable, d’infection profonde ou de perte de substance importante.
Par ailleurs, il n’existe pas de risque dégénératif connu (transformation maligne) associé à l’angiodermite nécrotique.
Combien de temps pour cicatriser ?
La durée de cicatrisation d’une angiodermite nécrotique est variable : elle dépend du terrain, de la précocité du diagnostic, et de la rapidité de mise en place d’une greffe cutanée. Avec une prise en charge adaptée, la greffe permet souvent une cicatrisation en quelques semaines. Sans greffe, l’évolution est généralement lente : plusieurs mois sont parfois nécessaires pour obtenir la fermeture complète de la plaie.
Un suivi spécialisé est recommandé jusqu’à cicatrisation complète pour prévenir la récidive.
Quelle prévention des récidives proposer ?
- Équilibration du diabète et de l’hypertension artérielle
- Crémage régulier des jambes
- Éviter les chocs (protection des jambes)
z
Cas cliniques et photos
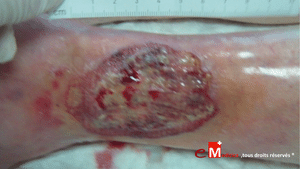
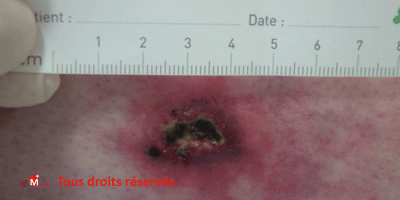
Illustrations cliniques : deux présentations contrastées d’angiodermite nécrotique
Cas clinique n°1 : une angiodermite nécrotique particulièrement récalcitrante
Cas clinique : une plaie rétive et évolutive
Un homme de 76 ans consulte pour une lésion
malléolaire externe droite, d’environ 1,5 cm,
apparue dix jours plus tôt après un traumatisme minime. La plaie est
d’emblée extrêmement douloureuse, s’étend de manière centrifuge et présente
une nécrose cutanée rapidement progressive. Le terrain est typique :
hypertension artérielle ancienne et diabète de type 2.
Un Doppler artériel ne retrouve pas d’artériopathie sévère, ce qui oriente
vers une angiodermite nécrotique. La lésion étant récente, une
greffe en pastilles est indiquée pour stopper la poussée et soulager la
douleur. La première semaine est favorable, mais dès la deuxième semaine, la
douleur réapparaît et la nécrose reprend, signe d’échec partiel.
Une électrostimulation est tentée avec un soulagement incomplet.
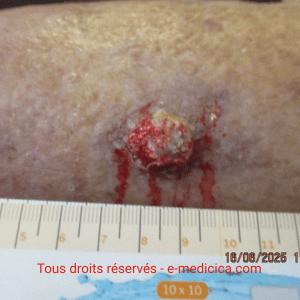
L’angiodermite continue pourtant de s’étendre. Peu après, la situation se
dégrade brutalement avec fièvre, creusement et
contact osseux. Le scanner confirme une ostéoarthrite,
imposant une prise en charge urgente par le chirurgien plasticien.
Deux lavages articulaires sont réalisés avec prélèvements, suivis
d’une antibiothérapie. Un lambeau est posé. Malgré une
évolution d’abord favorable, une nouvelle zone de nécrose apparaît à
J+15. Une greffe complémentaire est tentée, puis deux greffons en pastilles
sont appliqués en consultation suite à une nouvelle nécrose localisée.
Ce cas illustre la complexité extrême de certaines angiodermites
nécrotiques, parfois réfractaires malgré une prise en charge rigoureuse,
multidisciplinaire et rapidement initiée.
Enseignements du cas n°1
- Hyperalgie persistante : la réapparition de la douleur est un signal d’extension nécrotique.
- Greffe précoce parfois insuffisante : certaines angiodermites restent réfractaires malgré une stratégie optimale.
- Creusement + fièvre = urgence : évoquer une atteinte profonde (osteoarthrite, ostéite).
- Nécessité d’une équipe pluridisciplinaire : chirurgien plasticien, infectiologue, équipe douleur, infirmier expert.
- Évolution imprévisible : récidives de nécrose possibles même après lambeau et greffes multiples.
Cas clinique n°2 : une angiodermite nécrotique stabilisée par l’adaptation des soins
Cas clinique : une forme contrôlée par des soins ultra-doux
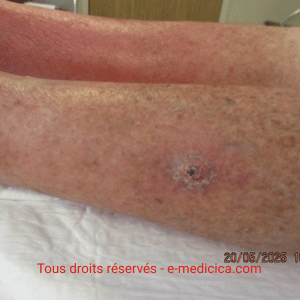
Une patiente octogénaire, hypertendue, présente une plaie très douloureuse
après un choc contre une table basse, au niveau du tibia gauche. La lésion,
d’environ 1 cm, est inflammatoire, lentement extensive, avec un
livedo périphérique.
Elle décrit des douleurs intermittentes intenses et de fortes douleurs
nocturnes. Les soins déclenchent eux-mêmes une douleur prolongée. Les pouls
sont difficilement perceptibles, et un bilan est programmé pour éliminer une
AOMI sévère ou une infection chronique.
Dans l’attente, des soins ultra-doux sont prescrits : arrêt du frottement,
simple tamponnement, et interruption de la détersion mécanique. Les
bilans ne retrouvent ni AOMI sévère ni infection.
Quinze jours plus tard, la patiente est nettement soulagée : la périphérie
n’est plus inflammatoire, et un début de cicatrisation apparaît.
Une pathergie induite par des soins trop agressifs est suspectée.
Les soins doux sont poursuivis. Devant un œdème associé, une
contention légère à faible élasticité est mise en place, bien tolérée,
sans réactivation de l’angiodermite. La plaie cicatrise en
deux mois, sans intervention supplémentaire.
Ce cas montre qu’une simple adaptation des soins locaux, respectant la
fragilité cutanée et limitant la pathergie, peut suffire à obtenir une
cicatrisation complète.
Enseignements du cas n°2
- Identifier la pathergie : les soins trop vigoureux aggravent l’inflammation et la douleur.
- Soins ultra-doux : tamponner au lieu de frotter, éviter la détersion mécanique.
- Exclure AOMI sévère et infection : bilans vasculaires et biologiques indispensables.
- Contention légère possible dans certains cas : utile sur l’œdème et bien tolérée si AOMI exclue.
- Approche minimaliste efficace : parfois, adapter les soins suffit à atteindre la cicatrisation.
Sources / Références
- Mansour M, Alavi A. (2019). Martorell ulcer: chronic wound management and rehabilitation. Chronic Wound Care Management and Research, 6, 83-88. https://doi.org/10.2147/CWCMR.S172427
- Senet P. (2016). Compression in hypertensive leg ulcer (Martorell’s ulcer). Veins and Lymphatics, 5(1), 5987. https://doi.org/10.4081/vl.2016.5987
- Mahé E, Montfort JB, Senet P, Nguyen-Chi HN. (2021). Prise en charge de l’angiodermite nécrotique en France. Phlébologie, 74(3), 85-89 : lien.
- Vuerstaeek JDD, Reeder SWI, Henquet CJM, Neumann HAM. (2010). Arteriolosclerotic ulcer of Martorell. JEADV, 24(8), 867-874. https://doi.org/10.1111/j.1468-3083.2009.03553.x
- Braun-Falco M, Kovnerysz E, Schliemann S, Dissemond J. (2020). Angiodermite nécrotique : un ulcère à connaître. Revue Médicale Suisse, 16(636), 636-641: lien.
- Körber A, Klode J, Al-Benna S, Wax C, Schadendorf D, Steinstraesser L, et al. (2011). Etiology of chronic leg ulcers in 31,619 patients in Germany analyzed by an expert survey. JDDG, 9(2), 116-121. https://doi.org/10.1111/j.1610-0387.2010.07535.x
- Abbade LPF, Miot HA, Orsini M, Rossi BM, Marques SA, Hamzagic F, et al. (2021). Consensus on the diagnosis and management of chronic leg ulcers. Anais Bras Dermatol, 96(3), 246-272. https://doi.org/10.1016/j.abd.2020.12.004
- Dissemond J. (2017). Chronic leg ulcers. Hautarzt, 68(8), 614-620. Lien
- Bertin A, Senet P. (2019). Ulcères veineux : lésions atypiques à ne pas méconnaître. Phlébologie, 72(4), 28-37 : lien.
Tout savoir pour prendre en charge l'angiodermite nécrotique
Suivez notre formation approfondie avec photos, protocoles de soins et de traitement.