Traitement de seconde ligne : le PRP pour les plaies chroniques
Le Plasma Riche en Plaquettes ou PRP est la fraction du sang qui possède une concentration en plaquettes au-dessus de la normale. Or, les plaquettes sont une source de facteurs de croissance impliqués dans la régénération et la croissance des tissus. Certains de ces facteurs favorisent la prolifération et la migration des cellules, d’autres, la synthèse de collagène, de la matrice extracellulaire, le remodelage, l’angiogenèse (néovascularisation), l’augmentation de la perméabilité capillaire, etc…(1)
En concentrant le plasma contenant des plaquettes, on va augmenter la quantité de facteurs de croissance et donc favoriser le processus de cicatrisation d’une plaie (2)(3)(4). Par ailleurs, le PRP semble avoir également des propriétés antibactériennes.
La technique
Le PRP peut être injecté le long de la bordure d’une plaie. Il peut aussi être appliqué sous forme de membrane dans la plaie. Cette membrane va libérer progressivement les facteurs de croissance dans la plaie.
L’injection et la membrane peuvent être associées.
Il n’est pas rare de tremper les greffons de peau dans le PRP avant la pose. On peut aussi allier l’injection de PRP à la réalisation d’une greffe.
Les indications
Plaies résistantes aux traitements conventionnels
Plaies d’artérite et du diabétique (5)(6)
Plaies de grande taille non greffable (réduction de taille pour permettre une greffe ultérieure) (3)
Greffes de plaies (7)
Petites plaies non greffables
Cicatrices atrophiques à risque d’ulcère
Plaies avec exposition osseuse, ou de tendon, avec lambeau de réalisation difficile (8)
Les contre indications
Plaie avec infection non maîtrisée
Plaie cancéreuse
Préparation du PRP
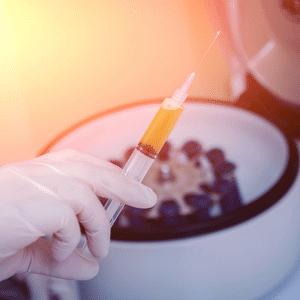
Une simple prise de sang (veineux) est effectuée sur la personne à traiter. Le sang est recueilli dans des tubes spéciaux. Ces tubes sont placés dans une centrifugeuse préprogrammée, qui va tourner pendant quelques minutes. La centrifugeuse a pour rôle de séparer la fraction plasmatique des globules rouges. On récupère ensuite la fraction plasmatique dans des seringues, pour l’injection, ou dans un récipient stérile pour réaliser une membrane.
Le traitement de la plaie
Il peut se faire aussi bien au bloc opératoire qu’en salle de soins.
Des antibiotiques peuvent être prescrits pour encadrer le geste. Le PRP est ensuite injecté autour de la plaie sous anesthésie légère (protoxyde d’azote), puis le pansement habituel est appliqué. Si une membrane a été réalisée, elle est découpée à la taille de la plaie puis appliquée. Un pansement adéquat est ensuite apposé. Le patient rentre à son domicile.
Le suivi
Il se fait à domicile par l’infirmière habituelle. En cas d’injection seule, il n’y a pas de surveillance particulière. En cas de membrane associée, l’infirmière passe tous les jours surveiller le pansement. Une consultation de contrôle a lieu 15 jours après. Il faut parfois deux à trois séances pour obtenir un résultat satisfaisant. En cas de greffe associée, les consultations sont plus rapprochées.
(1) Anthony P. Sclafani, MD; Steven A. McCormick. Induction of Dermal Collagenesis, Angiogenesis, and Adipogenesis in Human Skin by Injection of Platelet-Rich Fibrin Matrix. Arch Facial Plast Surg. Published online October 17, 2011. doi:10.1001/archfacial.2011.784
(2) Aprili, G., Gandini, G., Guaschino, R., Mazzucco, L., Salvaneschi, L., & Vaglio, S. (2013). SIMTI recommendations on blood components for non-transfusional use, 11(4), 611–622.
(3)Crovetti, G., Martinelli, G., Issi, M., Barone, M., Guizzardi, M., & Campanati, B., et al. (2004). Platelet gel for healing cutaneous chronic wounds. Transfusion and apheresis science: official journal of the World Apheresis Association: official journal of the European Society for Haemapheresis, 30(2), 145–151.
(4) Nandhagopal Vijayaraghavan1, Devi Prasad and all. , Department of Plastic Surgery, JIPMER, Pondicherry, India. Role of Autologous Platelet Rich Plasma (APRP) in Wound Healing. JSWCR 2014; 7(1): 23-28.
(5)Yotsu, R. R., Hagiwara, S., Okochi, H., & Tamaki, T. (2015). Case series of patients with chronic foot ulcers treated with autologous platelet-rich plasma. The Journal of Dermatology.
(6) Kontopodis, N., Tavlas, E., Papadopoulos, G., Pantidis, D., Kafetzakis, A., Chalkiadakis, G., & Ioannou, C. (2015). Effectiveness of Platelet-Rich Plasma to Enhance Healing of Diabetic Foot Ulcers in Patients With Concomitant Peripheral Arterial Disease and Critical Limb Ischemia. The International Journal of Lower Extremity Wounds.
(7) Tzeng, Y.-S., Deng, S.-C., Wang, C.-H., Tsai, J.-C., Chen, T.-M., & Burnouf, T. (2013). Treatment of nonhealing diabetic lower extremity ulcers with skin graft and autologous platelet gel: A case series. BioMed Research International, 2013.
(8) Valerio Cervelli, Lucilla Lucarini, Diana Spallone, Ludovico Palla, Gianfranco Marcello Colicchia, Pietro Gentile, and Barbara De Angelis. Use of Platelet-Rich Plasma and Hyaluronic Acid in the Loss of Substance with Bone Exposure. Advances in skin & wound care. Wound Care Journal (2011).