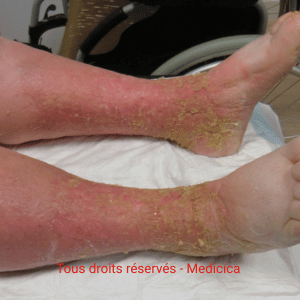
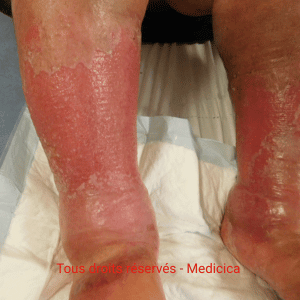
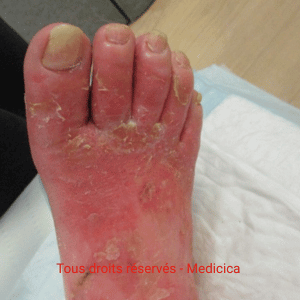
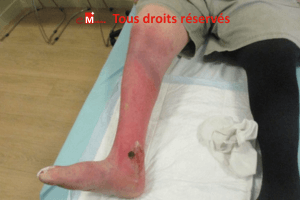
Plaies traînantes : facteurs de retard de cicatrisation version longue
Introduction
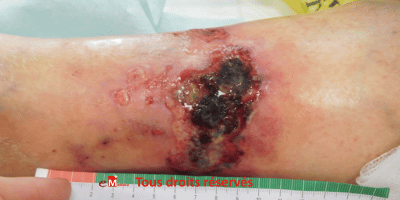
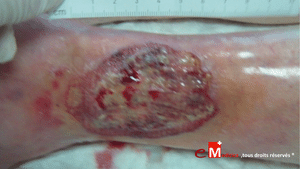
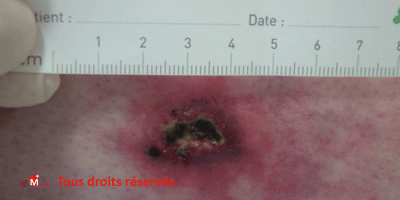
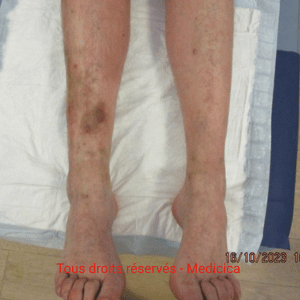
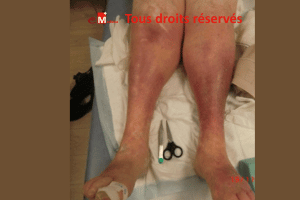
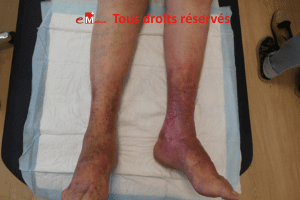
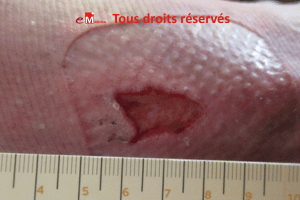
Une plaie traînante n’est jamais un simple échec de pansement. Elle traduit une interaction complexe entre l’étiologie sous-jacente, et les facteurs de retard de cicatrisation associés qu’ils soient systémiques, locaux, iatrogènes ou psychosociaux. Sans identification exhaustive et hiérarchisée de ces facteurs, la prise en charge reste symptomatique, avec des taux de cicatrisation souvent décevants et un coût clinique important.
Cet article propose une classification en quatre catégories et une check-list opérationnelle pour transformer la consultation d’évaluation en véritable levier thérapeutique.
Les 10 facteurs les plus fréquents
Dans les publications avec cohortes de plaies chroniques (ulcères de jambe, pied diabétique, escarres), ces facteurs reviennent systématiquement :
- Âge avancé et fragilité gériatrique.
- Insuffisance veineuse chronique
- œdème.
- Maladie artérielle périphérique et ischémie.
- Diabète et neuropathie.
- Obésité et sédentarité.
- Limitation de mobilité et dépendance fonctionnelle.
- Malnutrition et dénutrition.
- Insuffisance rénale ou cardiaque.
- Infection locale et biofilm.
- Tabagisme actif.
Les 10 facteurs les plus impactants sur la cicatrisation
- Infection locale sévère et biofilm.
- AOMI sévère
- Ostéite et os exposé, matériel exposé ou infecté.
- Insuffisance rénale sévère.
- Diabète compliqué.
- Grande surface, profondeur, et gangrène
- ancienneté de la plaie.
- Déclin fonctionnel et immobilité.
- Obésité.
- Malnutrition sévère.
Ces listes, issues de revues pronostiques et cohortes multicentriques, soulignent l’importance d’un dépistage systématique lors de la première consultation.
Vous disposez maintenant des bases essentielles pour structurer votre raisonnement face à une plaie traînante.
L’article complet qui suit développe la classification exhaustive des facteurs (plus de 60 items répartis en 4 catégories), les mécanismes physiopathologiques détaillés, les pièges cliniques à éviter (ex. sous-diagnostic d’ostéite, compression inappropriée), les algorithmes décisionnels et la check-list imprimable prête à l’emploi pour vos consultations quotidiennes.
Pourquoi cette classification est utile
Le but n’est pas seulement de lister des facteurs, mais de les hiérarchiser. Certains relèvent du terrain, d’autres de la plaie elle-même, d’autres enfin de la prise en charge.
En pratique, la priorité est de repérer ce qui conditionne le pronostic à court terme, ce qui empêche une stratégie locale efficace, et ce qui est modifiable rapidement.
Sans identification exhaustive et hiérarchisée des facteurs de retard, la prise en charge reste symptomatique, avec des taux de cicatrisation décevants (30-50% à 6 mois pour les ulcères complexes) et un coût socio-économique majeur.
Cet article plus complet propose une classification en 4 catégories (généraux, locaux, iatrogènes, psychosociaux), validée par la littérature, suivie d’une check-list opérationnelle. Objectif : passer d’un constat descriptif à un plan d’action ciblé.
Les grandes catégories de facteurs de retard
Facteurs généraux
- Âge.
- Ancienneté de la plaie.
- Tabagisme.
- Énolisme / alcoolisation chronique.
- Diabète.
- Obésité.
- Hypothyroïdie.
- Troubles circulatoires : insuffisance veineuse, lymphatique, artérielle.
- Douleur chronique et stress physiologique.
- Malnutrition / dénutrition.
- Carences protéiques et en micronutriments.
- Troubles neurologiques centraux ou périphériques.
- Troubles de la marche, déséquilibre, chutes.
- Cancer évolutif.
- Anémie.
- Hypoxémie.
- Défaillance d’organe : insuffisance cardiaque, respiratoire, hépatique ou rénale sévère.
- Démence, troubles neuropsychiatriques, syndrome confusionnel.
- Immunodépression : VIH, hémopathie, post-greffe, immunodépression liée aux traitements.
- Maladies inflammatoires systémiques, auto-immunes ou vasculitiques.
- Fragilité gériatrique et polymédication.
- Hygiène défectueuse.
Facteurs locaux
- Œdème.
- Infection locale ou profonde.
- Biofilm.
- Zone irradiée / antécédent de radiothérapie locale.
- Facteurs mécaniques : frottement, cisaillement, appui anormal, pression répétée, chaussage ou appareillage inadapté.
- Hyperbourgeonnement.
- Hyperkératose périphérique.
- Éversion, invagination ou enroulement des berges ; berges stagnantes.
- Plaie trop cavitaire ou géométrie défavorable.
- Facteurs cutanés périlésionnels : lipodermatosclérose, atrophie cutanée, sclérodermie, eczéma, dermite périphérique, macération, sécheresse.
- Fond de la plaie : fibrine, nécrose, hématome, débris, charge inflammatoire excessive.
- Exposition osseuse, tendineuse ou articulaire.
- Corps étrangers ou matériel résiduel.
- Insuffisance veino-lymphatique fonctionnelle au membre atteint.
- Raideur, ankylose de cheville, varus équin, dysfonction de la pompe musculaire du mollet.
- Hypoperfusion / ischémie locale.
Facteurs iatrogènes
- Pathergie.
- Douleur induite par les soins.
- Médicaments : AINS, corticothérapie au long cours, chimiothérapie, immunosuppresseurs, HYDREA®, NICORANDIL, anticoagulants / antiagrégants selon le contexte.
- Intolérances ou allergies de contact : pansements, bandes, crèmes, adhésifs, antiseptiques, topiques divers.
- Antiseptiques au long cours : cytotoxicité, altération de l’équilibre microbien local.
- Soins inadaptés : macération, absence de détersion, détersion excessive, méchage forcé, pansement inadapté à l’exsudat, compression inappropriée.
- Absence ou insuffisance de traitement étiologique : pas de compression si ulcère veineux, pas de décharge si plaie du pied, retard à revasculariser, retard diagnostique.
- Traumatisme répété par les soins ou par un matériel thérapeutique mal adapté.
Facteurs psychosociaux / comportementaux
- Isolement social.
- Précarité socio-économique, difficultés d’accès aux soins, au matériel ou aux transports.
- Faible / mauvaise compréhension du plan de soins.
- Mauvaise observance ou faible adhésion à la compression, à la décharge, aux pansements ou au suivi.
- Refus de soins ou épuisement thérapeutique.
- Anxiété, dépression, syndrome de stress chronique.
- Troubles du sommeil.
- Douleur avec retentissement fonctionnel, émotionnel ou comportemental.
- Sédentarité, évitement de la mobilisation, perte de confiance à la marche.
- Conduites addictives persistantes : tabac, alcool, autres substances.
- Contexte familial ou environnemental défavorable : absence d’aidant, logement inadapté, difficultés d’hygiène, surcharge domestique.
Raisonnement clinique en consultation
La consultation d’évaluation doit suivre un fil logique : confirmer l’étiologie principale, repérer les facteurs de retard majeurs, puis définir ce qui est modifiable à court terme. Cette hiérarchisation évite de disperser la prise en charge et permet de gagner du temps sur les situations complexes.
Étapes pratiques
- Poser le diagnostic étiologique principal.
- Repérer les facteurs prioritaires : ischémie, infection, os ou matériel exposé.
- Identifier les freins modifiables : compression, décharge, nutrition, tabac, douleur, observance.
- Programmer une réévaluation à 4 semaines avec mesure objective.
Check-list de consultation
La check-list permet de formaliser le recueil, de standardiser la consultation et de faciliter la transmission entre professionnels.
| Facteur | Présent / Absent | Impact | Action |
|---|---|---|---|
| Âge | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Diabète | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Insuffisance veineuse / artérielle | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Infection / biofilm | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Os ou matériel exposé | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Obésité | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Dénutrition | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Tabagisme | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Non-adhésion / difficultés psychosociales | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important | |
| Douleur importante | ☐ Oui ☐ Non | □ Faible □ Modéré □ Important |
Conclusion
La réussite de la prise en charge d’une plaie traînante repose sur la capacité à voir au-delà de la plaie elle-même. Plus la recherche des facteurs de retard est structurée, plus la stratégie devient efficace, rapide et reproductible. La consultation d’évaluation n’est pas seulement un constat : c’est un acte de triage clinique et un point de départ thérapeutique.
Cliquez sur l’image ci dessous pour télécharger ma check list complète pour vos consultations d’évaluation (format pdf ):